Stål: Herding og varmebehandling
/Av alle de ting vi kan gjøre med stål, er herding desidert det viktigste og mest nyttige. Men ytterligere varmebehandling er vel så viktig.
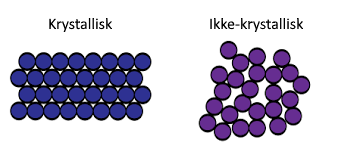
Som vi nå har forstått så er en finere kornstruktur, med mye fastlåst karbon, hardere - og dette oppnår vi ved å herde stålet, med andre ord, bråkjøle det. Men det er ikke nødvendigvis sterkere.
På samme måte som glass, hvor det bygges opp sterke spenninger i materialet dersom det ikke kjøles sakte ned, vil et martensittisk stål være svært anspent og ha lyst til å bryte seg fri fra sin smertefullt fastlåste tilstand. Derfor skal det ikke mye til før herdet stål knekker, knuser eller brister. Noen applikasjoner krever slikt knallhardt stål, men i det store og det hele er stål i denne tilstanden på mange måter nesten like ubrukelig som det var før vi herdet det.
I denne moderne informasjonsalderen henter jeg mye av min kunnskap fra engelske kilder, og det hender at det medfører noe forvirring, spesielt når ord som ligner på hverandre - som logisk og statistisk sett kunne bety det samme - ikke gjør det. Det kan være farlig å anta ting, og det er ikke første gangen jeg har forsøkt å finne informasjon om et konsept på engelsk, hvor jeg etter litt hodebry finner ut at det jeg søkte på ikke har noe med det jeg trodde det hadde. Det er derfor jeg pleier å legge ved tingenes engelske navn i innleggene mine slik at det blir enklere for andre å gjøre sin egen “research” selv, videre på det språket det finnes mest informasjon om ting på.
Et godt eksempel er når det kommer til navn på varmebehandlinger på norsk, kontra engelsk.
Herding, anløping, normalisering, utgløding, settherding og flammeherding er navn på ulike varmebehandlingsmetoder.
Herding gjør stålet hardere. Men hva er anløping, normalisering og utgløding?
På engelsk heter herding hardening, eller quenching, som betyr mer selve handlingen å dyppe glødende stål i en kjølevæske. Forvirringen inntraff når man kommer til anløping, der det ikke er for langt å strekke seg til å anta at det vil være annealing på engelsk. Men det betyr ikke det. Her er en liste over korrekte oversettelser:
Herding -> Hardening/quenching
Anløping -> Tempering
Normalisering -> Normalising (dette derimot gir mening, er det rart man blir forvirret i blant)
Utgløding -> Annealing
Settherding -> Case hardening
Flammeherding -> Colour case hardening
Vi skal ta for oss disse i rekkefølge.
Herding
Herding er ikke herding, og materialets egenskaper kan endres dramatisk med ulike herdemetoder.
For det første er det vikitg å la stålet varme seg sakte opp. Et større stykke stål krever mer oppvarmingstid for en jevnere, mer helhetlig oppvarming, der kjernen skal ha samme temperatur som de mer ytterliggende lag til enhver tid og tynnere deler gjennomvarmes raskere enn tykke (duh…), og stålet må gis tid til å gjennomgå faseendringene sine på vei opp, på en samlet måte.
Dersom det brukes en ovn er det tilstrekkelig å legge arbeidsstykket i ovnen etter at den har nådd herdetemperatur, men å legge det inn før ovnen skrus på, og la stålet varmes opp med ovnen er enda bedre. Dersom det benyttes blåselampe eller gassflamme, er det ekstra viktig å ta seg god tid med oppvarmingen. Man kan selvsagt ikke forvente å sitte i en halvtime å varme opp noe for hånd, men å bombardere arbeidsstykket med varme til det gløder er ikke å anbefale. Det er også særlig viktig å påse at arbeidsstykket ikke overopphetes lokalt, særdeles utsatt er tynne deler.
Stålet må også holdes ved herdetemperatur i nødvendig mengde tid før det kjøles for å sikre at alt stålet har fått tid til å gjennomgå faseendringen. Med herdetemperatur menes det den temperaturen stålet bør ha når det bråkjøles.
Hvor lenge stålet bør være ved herdetemperatur og hvilken temperatur som er optimal varierer voldsomt mellom ståltyper og fysiske dimensjoner på stykket; konsulter leverandøren av stålet, de har skjemaer og diagrammer for slikt, men som en tommelfingerregel skal stålet hvile på herdetemperatur én time per tomme. I know, I know, vi avskyr tommer, men det er ihvertfall slik regla går. Å bare varme opp stålet til det gløder for så å bråkjøle det, funker, men der er langt fra optimalt og man kan se ganske store endringer i egenskaper kun på hvor lenge stålet har blitt varmet opp og ligget ved herdetemp.
Når det kommer til å finne riktig temperatur så vet vi at karbon senker smeltepunktet til stål, så et stål med høyere karboninnhold krever lavere herdetemperatur (opp til 0,8% karbon). Man bør som sagt høre med fabrikanten, men dersom dette ikke er tilgjengelig, og vi vet karboninnholdet, kan vi se på fasediagrammet for å finne et høvelig brukbart substitutt:
Vi vil ha austenitt, altså må vi inn i det skraverte området over det nedre kritiske punkt for stålet A1, ca 723°C (for eutektoid stål), men ikke så høyt at det begynner å smelte (som igjen kommer an på karboninnholdet, ca. 1100-1500 °C, se linje Acl). For hypo-eutektoide og hyper-eutektoide ståltyper må vi også over deres respektive øvre kritiske punkt A3 og Acm respektivt, ellers havner vi i et inter-kritisk faseområde der noe av stålet er omgjort til austenitt, men ikke alt. Typiske herdetemperaturer for stål ligger på 800-900 °C, over det øvre kritiske punktet for en gitt ståltype, men det er ikke nødvendig å gå mye over; det er hensiktsmessig å “ri“ på denne linjen A3-Acm. Vi kan også se Curie-punktet ved A2.
Metningsgrensen for karbon i austenitt er som nevnt i tidligere kapittel 0,83% (ved (og under) den nedre kritiske temperaturen - hensikten med oppvarmingen er jo å tillate mer fritt karbon i løsningen enn det normalt er plass til). Over dette forekommer det cementitt, frem til neste metningsgrense (2,06%) der karbonet ikke vil binde seg og ikke lage mer karbid, men binde seg til seg selv og lage granuler av grafitt (ledeburitt).
Selv om karbonet senker nødvendige temperaturer for å endre stålet, så er karbonbindinger (karbider) selv veldig vanskelige å bryte opp, så når det er overflod av karbon i stålet kreves det mer varme å gjøre om alt materiale til en homogen blanding av austenitt.
Det er her viktig å presisere at fasediagrammet kan ansees å ha 2 møtepunkter, El og Es der El er det eutektiske punktet, siden det omhandler smeltepunkt, mens Es er det eutektoide punkt som representerer fase-likevekt i fast form. Når det snakkes om stål i forhold til herding sies det å være hypo-eutektoid til venstre for Es og hyper-eutektoid til høyre.
Men tenk ikke mer på det, for på tross av all teorien bak krystallformasjon og slikt i forrige kapittel, er egentlig alt til høyre for 2,06% karbon på diagrammet uinteressant for oss akkurat nå.
Dersom vi ikke vet karboninnholdet i stålet er det mulig å utføre noe som kalles en “spark test“. Det går ut på å slipe en bit av stålet som skal identifiseres på en slipemaskin og observere gnistene som produseres. Lange gnister som forsvinner ut i ingenting betyr et lavt karboninnhold, mens korte, ujevne gnister som ender i små fyrverkeri-lignende eksplosjoner betyr generelt et høyere karboninnhold, men det er mange andre karakteristikker ved gnisten som kan fortelle noe om materialet, som farge, lengde, størrelse og form. Det er også mange legeringselementer som endrer gnisten. Mer informasjon om dette her.
Som sagt er det martensitt vi ønsker å oppnå når vi herder. Martensitt oppstår av en diffusjonsløs transformering (krystallene rekker ikke å spytte ut overflødig karbon) fra austenitt ved rask nedkjøling til en temperatur på ca 220° (M start) eller lavere (avhengig av ståltypen). En lavere temperatur som nåes raskere sikrer at en større andel av austenitten blir omdannet til martensitt. Transformeringen er nesten umiddelbar. Som en liten påminner har jeg brakt frem vår gamle venn TTT-diagrammet:
Jo mer av stålet som er austenitt (maksimalt opptak av karbon i jernkrystallene, mer enn det som er “lov“ ved lavere temperaturer) når det bråkjøles, jo mer helhetlig martensitt oppnår vi. Dersom stålet er hyper-eutektoid, altså en overflod av karbon, vil stålet i det inter-kritiske sjiktet ha klumper av cementitt. Dersom en slik blanding bråkjøles vil, i tillegg til å fange karbon i austenitten, cementitten heller ikke har tid til å krystallisere seg normalt, og vil danne nål-lignende strukturer som kalles en acikulær formasjon, lignende bainitt. Denne er veldig hard og egner seg godt til knivsegger og lignende. Det er ofte hensiktsmessig å ha litt fri cementitt når man herder også, så som en generell regel bør stål med et karboninnhold over 1% herdes fra under det øvre kritiske punktet (altså mens det er i det inter-kritiske sjiktet, under linje Acm), mens stål under 0,9% karbon bør herdes fra over det øvre kritiske punktet (100% austenitt).
Dersom man ikke har tilgang på en kontrollert oppvarming med temperaturmåling, som en herdeovn, går det an å anslå temperaturen basert på fargen stålet har. Dette er ikke eksakt, men funker til generell bruk:
Herdemedier
Vann er det enkleste og vanligste kjølemediet. Men det er også det mest ‘brutale‘. I motsetning til olje eller saltlake, som er to andre utbredte herdemedier som er litt ‘snillere‘. De gir en litt mer utstrakt nedkjølingskurve.
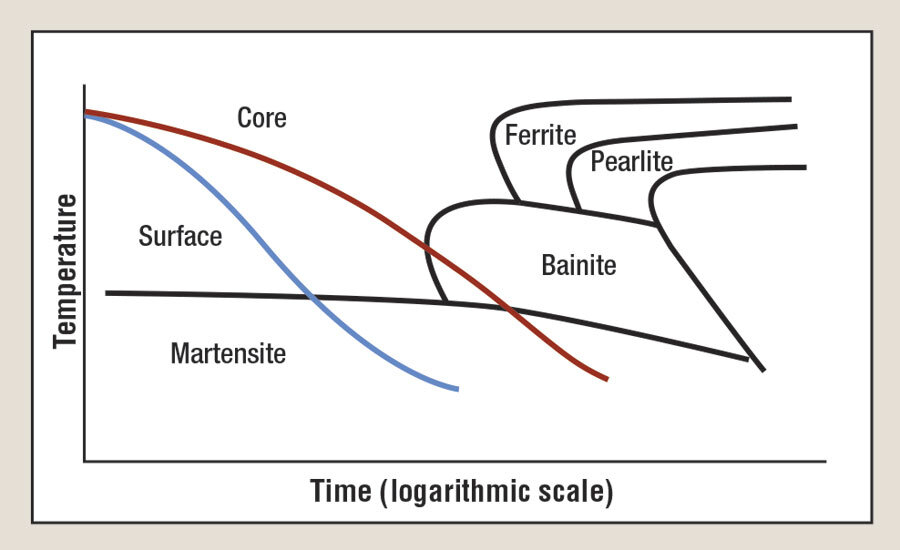
Det er et uunngåelig faktum at tykkere deler holder lenger på varmen, og er derfor vanskeligere å herde helt gjennom. Man vil oppnå martensitt i det yttere skall, men kjernen, som åpenbart ikke er i direkte kontakt med kjølemediet, kan i tilfellet av svært tykke deler kjøle seg ned såpass sakte at det nødvendigvis må gå gjennom et stadie som danner perlitt eller bainitt. Men detter er ikke alltid en dårlig ting. Martensitt er særdeles hardt, men skjørt. I tilfellet av håndholdte verktøy, som kniver, meisler, hoggjern og annet verktøy som må være skarpt er det bra å ha en mykere, seigere, kjerne som er mer motstandsdyktig overfor slag og støt, mens den skjærende delen er hard og holder en skarp egg lenge. Men det er også noen ganger man vil ha noe med en gjennomgående martensittisk struktur.
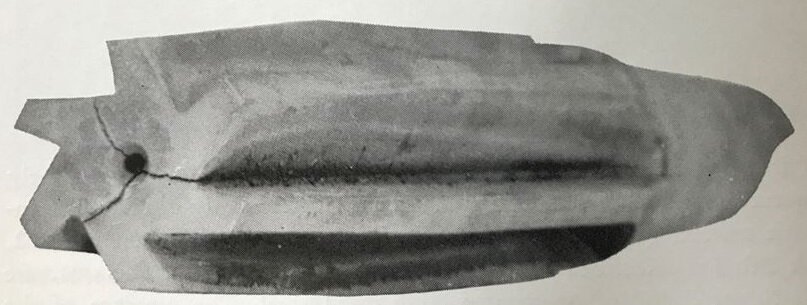
Dersom noe skal herdes, får så å slipes til, kan det hende man sliper seg ned til denne mykere kjernen, dersom det ikke er gjennomherdet:
Bråkjøling
Så hvordan bråkjøler man? Er det bare å dyppe en glødende bit stål i vann på måfå? Vel, det er et bedre utgangspunkt enn mye annet, men det er et par ting som må tas hensyn til ved selve prosessen av å dyppe stålet i herdemediet.
For det første vil det å putte glødende stål i vann selvsagt skape vanndamp. Vannet som er i kontakt med stålet, og i umiddelbar nærhet, vil varmes opp raskt og lage en isolerende hinne av damp rundt arbeidsstykket; dette hindrer effektiv kjøling og hemmer prosessen. Luft er en særdeles dårlig termisk leder så vi må flytte stålet rundt i badet for å fjerne det fra det nå oppvarmede vannet og dampen som hindrer god termisk kontakt. Hvordan noe skal flyttes rundt i et herdebad er en kilde til diskusjon, men flyttes må det.
Å føre det rundt i en sirkel er en logisk slutning og enkel metode man kan tenke seg å bruke. Noen sverger til å føre det rundt i et åttetall, men dette er ikke nødvendig. Men det viktige er å ikke føre det rundt for fort. Dersom stålet virvler gjennom badet vil et undertrykk skapes i turbulensen bak det der damp vil bli fanget og hindre god kjøling. Samtidig må det beveges lett opp og ned om mulig, slik at bevegelsen danner en heliks. Trikset er å gjøre det SAKTE. Ikke så sakte at dampen forblir i nærheten av stålet, men ikke så fort at det skapes strømmer rundt det.
Pilene på bildet beskriver vannstrømmen, ikke stålets bevegelse, og vi kan se at det oppstår en sone med dårligere kjøling i punktene A.
Å herde i saltlake gir en litt snillere og jevnere kjøling, men derav også mindre hardhet. Det samme gjelder herdeolje/mineralolje, som er spesielt laget for å ha et høyt selvantenningspunkt. Olje forminsker problemet med damp (men fjerner ikke helt), men stålet må fremdeles føres rundt for å stadig ha det i fersk, kald olje.
Dersom noe langt og tynt, eller snodig formet stål skal herdes, er det enda viktigere å være var på kjølemetoden. Det er å forvente at stålet deformerer seg noe når vi herder det. Det vil nødvendigvis krympe slik at det kan skapes skjevhet i arbeidsstykket, spesielt dersom det ikke er nøyaktig symmetrisk eller ikke kjøles likt på begge sider. Dette er spesielt et problem i filer og sverd og lignende, der kjølemetoden til og med kan brukes for å rette ut skjevheter ved å bruke denne kunnskapen riktig. Men stort sett, ved herding av lange biter er det viktig å senke dem ned i badet hengende rett ned, og kun bevege dem opp og ned, med svært begrenset bevegelse sideveis.
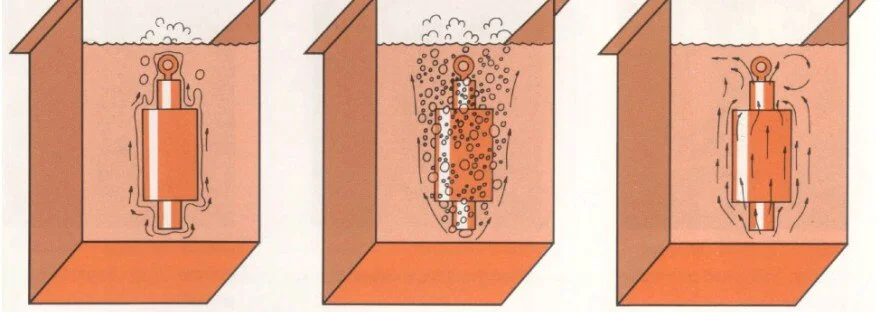
På diagrammet til venstre kan vi se de tre hovedstadiene i nedkjølingsprosessen:
Stadie A: Umiddelbart etter nedsenking vil mediet i kontakt med stålet fordampe og en hinne av gass dannes rundt objektet som hindrer effektiv kjøling. Ingen væske kommer nå i kontakt med stålet og kjøleeffekten senkes drastisk. Dette er en uønsket tilstand.
Stadie B: Etter kort tid vil mediet rundt stålet begynne å koke eller på andre måter oppføre seg turbulent slik at gasshinnen blir tidvis brutt opp og gir mer effektiv kjøling. Herdemediet kommer lettere til, men blir raskt dyttet vekk igjen av fordampningen. Gassboblene blir fraktet vekk fra stålet av konveksjonsstrømmer og slik oppstår en naturlig strøm av nytt herdemedie og en sirkel av mer effektiv kjøling. Den hurtige nedkjølingen i dette stadiet bringer raskt overflaten av stålet ned til, eller under, kokepunktet til mediet. Dette er det viktigste og meste kritiske stadiet i nedkjølingen.
Stadie C: Fordampning og gassdannelse opphører. Overflaten er nå under kokepunktet til mediet, men avhengig av tykkelsen på objektet kan kjernen være betraktelig varmere. Kjøling skjer via konveksjon og termisk ledelse gjennom væsken. Kjølingen er tregere.
Det er viktig å notere at kurven og beskrivelsene over gjelder for et stillestående arbeidsstykke, og kjølingen kan forbedres med bevegelse i mediet som forklart øverst, men prinsippene er de samme og stadiene vil oppstå i én eller annen grad uavhengig av kjølemetode eller kjølemedie.
Det er flere faktorer som bidrar til å endre egenskapene og effektiviteten til herdemediet:
1. Temperaturen til kjølemediet:
I vann og saltlake vil den initielle kjøleevnen synke når temperaturen til mediet øker. Et medium som er nærmere sitt kokepunkt vil raskere fordampe og det forenkler og forlenger stadie A der det oppstår en damphinne.
I olje ser vi det motsatte. En økning i temperatur i olje senker viskositeten og dermed gjør det mer “flytende“ som bidrar til enklere forming av strømmer og raskere fjerning av varme fra stålet. Det oppstår allikevel en raskere formasjon av gasshinnen når oljen er varmere, så det er en balansegang. Optimal temperatur for oljebad ligger på 50-80 C°.
2. Kokepunkt:
Jo lavere kokepunktet til mediet er, jo raskere skapes gasshinnen rundt stålet som forlenger stadie A, som gir tregere kjøling. Medier med høyere kokepunkt gir en mer effektiv kjøling.
3. Varmekapasitet:
Hvor mye energi som kreves for å øke temperaturen i en gitt enhet væske, én enhet temperatur, er varmekapasiteten til væsken. F.eks. kreves det 1 kalori for å øke temperaturen i ett gram vann 1C°. Jo lavere varmekapasitet, (altså jo mindre energi væsken kan holde før temperaturen går opp), jo raskere vil væsken varmes opp og forverre kjølevnen. Dersom det er lite kjølevæske i badet, eller mange ting skal herdes, er det nødvendig å bruke en væske med høy varmekapasitet eller ha god kjøling til kjølevæsken.
4. Fordampningspunkt:
Varmen som kreves for å omgjøre en enhet væske om til gass ved en konstant temperatur. En væske med lavt fordampningspunkt forlenger stadie A, men varmer ikke opp resten av væsken like fort som en væske med høyere fordampningspunkt.
5. Termisk ledeevne til mediet:
En væske med rask termisk ledeevne overfører og fordeler varmen fra stålet til badet raskt, som forbedrer kjøleevnen.
6. Viskositet:
En mer viskos væske fordeler varmen fra stålet tregere rundt i herdebadet og forlenger gasshinne-stadiet.
7. Sirkulasjon i mediet:
Som nevnt tidligere så vil det å bevege delen rundt i herdebadet fjerne gasshinnen ettersom den dannes og drastisk forkorte stadie A, og mer eller mindre direkte gå til stadie B.
Stadie A, B of C, fra venstre til høyre.
Noen viktige momenter ved nedsenkningen:
En del som har betraktelig tynnere eller tykkere seksjoner bør nedsenkes med den tykke seksjonen først. Eller det kan monteres en varmebuffer på de tynne seksjonene slik at de oppfører seg noenlunde likt som de tykkere seksjonene.
Lange og tynne deler skal nedsenkes vertikalt.
Runde deler som ringer skal nedsenkes aksialt, d.v.s. liggende, med aksen vinkelrett på herdebadet.
Tynne og flate deler skal nedsenkes “stående“ med kanten først. Begrens sidelengs bevegelse.
Deler med konkave former må nedsenkes enten sidelengs eller med den konkave formen opp for å hindre at gasshinnen blir fanget i denne formen.
Små hull i deler burde tettes.
Dersom noe veldig tynt og flatt skal herdes bør det benyttes en fikstur.
Det er som sagt et uungåelig faktum at overflaten kjøles ned raskere enn kjernen. Ofte er dette uproblematisk, men det er viktig å være obs på dette fenomenet dersom noe skal være gjennomherdet.
I tillegg til å hindre gjennomherding, kan dette også skape spenninger mellom det kalde harde yttre og det varmere indre.
Selv om en rask nedkjøling som oftest er ønskelig så er det også noen ganger hensiktsmessig å nesten dulte borti S-kurven, for å oppnå maksimalt med martensitt uten å utsette arbeidsstykket for dette altfor voldsomme termiske sjokket som kan lede til sprekker o.l., og det finnes et par metoder utviklet for å oppnå dette:
Varmherding:
Varmherding (eng: austempering) er en herdemetode som brukes (hovedsakelig i industri) når eliminering av dimensjonal deformasjon er viktigst. Det er en prosess som benyttes på middels- til høy-karbon stål, og produserer nedre bainitt. En ikke-lammelær, men allikevel blandet, nål-lignende struktur, som minner om en blanding av perlitt og martensitt, men med større korn og bestående av cementitt og ferritt. (Hovedforskjellen på nedre og øvre bainitt er måten cementitten sammenblander seg med ferritten. Nedre bainitt, som oppstår ved lavere temperaturer har mer av karbonet som karbid inneklemt i ferritten, mens i øvre bainitt, som oppstår ved høyere temperaturer, er de to formasjonene renere og separert mer lagvis.) Produktet kalles noen ganger ausferritt.
Metoden går ut på å bråkjøle austenitten til rett over punktet der martensitt starter å oppstå, for så å holde temperaturen over tid slik at bainitten kan oppstå. Dette er hardere enn perlitt, men ikke fullt like hardt som martensitt. Det er seigere og mer stabilt, men fortsatt hardt nok til bruk i mange applikasjoner.
Krever vanligvis ikke ytterligere behandling etter avkjøling.
Stegherding:
Stegherding (eng: martempering) er en herdemetode som benyttes når det er viktig å unngå sprekker og minimerer deformasjon men som allikevel produserer martensitt. Det går ut på, som man kan se på diagrammet, å bråkjøle austenitten til rett over startpunktet for martensitt, men la det hvile der i en liten periode, men ikke så lenge at det begynner å forme bainitt, for så å bråkjøle det videre helt ned gjennom martensitt-sjiktet. Dette senker det termiske stresset på stålet når det går gjennom martensitt-formasjonen og senker som sagt sannsynligheten for sprekker og deformasjon.
Stålet bråkjøles i enten et oppvarmet oljebad, flytende bly eller flytende saltbad og holdes der i en periode, for så å overføres til et konvensjonelt herdebad.
Krever vanligvis anløping etter herding.
Vanlige årsaker til sprekker og brister ved herding:
Kjølevæsken brukt er for brutal.
Ståltypen brukt egner seg ikke til herding eller herde-metoden brukt.
For lang tid mellom bråkjøling og anløping.
Uegnet form; skarpe overganger, hull, mangel på radier, usymmetrisk.
Dårlig nedsenkning eller tilføring av kjølemediet.
Eksisterende sprekker/defekter etter maskinering.
Lokal over-karburisering eller oksidasjon ved oppvarming.
Overoppheting eller for mye tid ved høy temperatur. Kornene i stålet kan ha reformert seg og grodd til størrelser som skaper større potensielle bruddpunkter.
Anløping
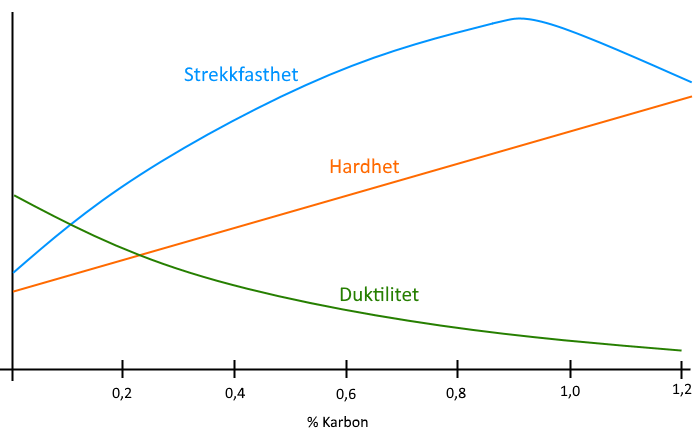
Anløping er en etterbehandling som brukes på herdet stål for å gjøre det “sterkere” - mer motstandsdyktig mot slag og last- på bekostning av litt hardhet.
Herdetemperaturen til stål er mer eller mindre kun avhengig av karboninnholdet, mens anløpingstemperaturen avhenger hovedsakelig av stålets planlagte bruk. En fil, som ikke skal utsettes for mye sjokk trenger nesten ikke anløpes i det hele tatt, mens en fjær må anløpes kraftig.
Som sagt så består herdet stål av martensitt, som er en veldig hard og skjør struktur. Ved å varme opp stålet til over martensittgrensen, ca. 200 C°, og opptil rundt 350 C°, kan vi “mykne“ opp krystallene og frigjøre stress fra strukturen. Jo høyere temperatur, jo sterkere blir stålet, på bekostning av hardheten.
Denne grafen er ikke en fasit, kun representativ for konseptet.
Styrke i denne forstand er nokså vagt, og kan deles inn i mange forskjellige former, men stort sett regnes det som motstandsdyktigheten mot brudd.
I sakens rette forstand så senker vi Young’s modulus ved å anløpe, slik at stålet blir mer tilbøyelig 😉 til å vri, bøye eller strekke seg enn å knekke under en påkjenning/last. Det er jakten etter den gylne middelvei her som er tingen når det kommer til kutteverktøy f.eks.. Vi vil ikke gjøre stålet for bløtt igjen heller, slik at det ikke er i stand til å holde eggen skarp, men vi vil styrke det slik at det ikke knekker tvers av.
Produktet av denne prosessen kalles for anløpt martensitt (eng: tempered martensite).
Hvilken temperatur og tid som er best egnet til hvert enkelt tilfelle er som sagt anhengig av bruken, men også litt av karboninnholdet og størrelsen. Et høy-karbon stål vil naturligvis bli hardere enn et stål med mindre karbon nå de herdes, så en lik anløpingsprosess brukt på begge stålene vil resultere i ulike egenskaper. Hvor lenge stålet skal holdes i varmen er også en faktor. Dette kan variere fra minutter til timer, avhengig av størrelse og bruk.
Før i tiden, da det ikke fantes herdeovner eller termostater, var det vanskelig å vite eksakte temperaturer, og smedene var dermed nødt til å anslå anløpningen basert på fargen stålet fikk.
Disse fargesjiktene kommer av at ettersom stålet varmes opp blir det mer og mer reaktivt med oksygenet i luften, og det dannes et oksidlag på stålet, hvis tykkelse avhenger av temperaturen, og er forøvrig ganske nøyaktig og pålitelig, og vil endre hvilke bølgelengder av lys som reflekteres og hvordan disse oppfører seg.
Dette krever at stålet er rent for herdeskall og relativt blankt. Det må også være fritt for fett og olje.
I dag brukes dette lite i industri, men er fremdeles brukt som rustbeskyttelse eller rett og slett som en kosmetisk finish.
Det er nesten alltid best å anløpe i en ovn over lengre tid enn å “blåanløpe” med flamme. For at anløpningen skal gi så mye effekt som mulig så må stålet igjen ligge og få godgjøre seg. Varmebehandling av stål er ikke en ting som bør gjøres i hast hvis man vil ha best mulig resultat. Regelen for anløping er den samme for herding. Én time per tomme. Eller 25 minutter per centimeter om du vil, men allitterasjonen i den første gjør den enklere å huske.
Når det er sagt så er det mulig å oppnå en tilsvarende anløping med høyere temperatur over en kortere periode som en lavere temperatur holdt over lengre tid.
Dersom vi bruker flamme og anløper til farge oppstår, og stålet er gjennomherdet, kan vi ende opp med å bare mykne opp skallet, men beholder en hardere kjerne, noe som nesten universalt er en dårlig kombinasjon.
Dersom ujevn anløpning er ønskelig, som i et verktøy som må være særdeles skarpt på tuppen, men trenger et langt skaft som tåler litt juling, kan det være fordelaktig å bruke flamme. Vi kan f.eks. varme opp skaftet og “ri“ varmen så vidt ut til tuppen slik av vi får en jevn behandling og overgang.
Dersom direkte varme ikke kan brukes, enten grunnet veldig delikate deler eller fare for lokal overanløpning, kan delen monteres i en fikstur eller skaft som varmes opp og leder varmen inn i delen.
Anløpning burde utføres så raskt som praktisk mulig etter herdeprosessen for å minimere sjansen for sprekker og brist. Hvis det anløpes med flamme så sørg for å bruke en ren flamme som ikke karburiserer eller dekarburiserer (oksiderer) overflaten unødig, som butan eller godt innstilt oxy-acetylen.
Det finnes andre oppfinnsomme måter å anløpe på også som i et saltbad, oljebad, blybad eller sponbad.
Bilder er fra Clickspring sin YouTube kanal.
Stålet behøver ikke være herdet for å oppnå disse fargene.
Vanlige (veiledende) anløpningstemperaturer for ulike applikasjoner:
Dette avhenger selvsagt at det blir brukt riktig type stål til bruken, resultatet av de ulike temperaturene vil som sagt være avhengig av karboninnholdet og legeringen.
Normalisering og utgløding
Normalisering og utgløding (eng. normalising og annealing, respektivt) er nokså like prosesser i bunn og grunn, men avviker noe i utførelse og gjøres av ulike grunner. Begge behandlingene går ut på å varme opp stålet til 20-50 °C over sitt øvre kritiske punkt for så å la det kjøle seg sakte ned.
I all hovedsak så brukes utgløding for å mykne opp allerede herdet stål, enten det er bråkjølt med vilje eller arbeidsherdet gjennom bearbeiding. Mens normalisering brukes hovedsakelig for å rekrystallisere stålet etter mekanisk bearbeiding som har strukket, vridd eller på andre måter innført spenninger, dislokasjoner og ubalanse i kornstrukturen. Målet med begge prosessene er å få stålet tilbake til en mykere og mer duktil tilstand som lettere kan bearbeides videre.
For at disse prosessene skal lykkes er det avgjørende at det blir gjort i en ovn med temperaturkontroll. Det er spesielt viktig å la disse behandlingene få den temperaturen og tiden som kreves for at korrekt rekrystallisering skal finne sted (selve temperaturen er ikke kritisk innenfor +/- 10°C). Dette er særdeles viktig for utgløding, som bør gjøres med veldig sakte nedkjøling for å tillate at den går gjennom perlitt-stadiet. Samme regelen for tid gjelder her også, men jo høyere karboninnhold , jo viktigere er det med sakte nedkjøling og lengre varmetid. Normalisering kan tas ut og luftkjøles etter nødvendig varmetid i ovnen. Det vil bli noe hardere enn full utgløding, p.g.a. den raskere nedkjølingskurven, men det er vanligvis ikke et problem.
Normalisering kan ha en raskere nedkjøling men må ha høyere øvre temperatur enn utgløding ettersom den skal flytte og endre litt på eksisterende, men forstrukkede korn, mens utgløding endrer bare den interne krystallstrukturen, som krever lengre nedkjøling. Alt vi gjør med normalisering er egentlig å tilbakestille flytegrensen til materialet (grensen mellom elastisk og plastisk deformering) i utsatte områder, mens utgløding tilbakestiller hardheten og øker duktiliteten og formbarheten.
Grunnen til at grafen ser ut som den gjør - at utgløding av hyper-eutektoid stål vanligvis ikke går over den øvre kritiske grensen Acm - er fordi temperaturen som kreves for å produsere homogen austenitt blir fort veldig høy, som drastisk øker sjansen for at krystallene gror (som er uønsket) og dekarburisering av stålet. I det inter-kritiske sjiktet for hyper-eutektoid stål vil det være austenitt som har formet seg fra martensitten og litt mer av karbonet blir sugd opp fra den pre-eksisterende cementitten i løsningen. Denne cementitten vil ikke bli affektert noe ytterligere enn at den vil bli svakt fortært og inklusjonene av den øvrige cementitten er ikke av kritisk skade for resultatet. Å austenittisere stålet er målet, men i motsetning til normalisering - hvor målet er å reorganisere deformerte korn - prøver vi kun å endre krystallstrukturen i kornene som de er ved utgløding.
Over ser vi 0,18% karbon stål (a) og 0,95% karbon stål (b) , begge utglødet ved 900°C. Legg merke til den store mengden ferritt (hvitt) i a, med inklusjoner av perlitt (skraverte felt), mens i b er strukturen en komplett perlittisk struktur med noen små cementitt-inklusjoner. Dette viser hvordan et hyper-eutektoid stål kan reformeres til et lett bearbeidet materiale, samt at det viser en interessant sammenstilling mellom et “umettet“ stål og et “mettet“ stål. Stål b vil være veldig mye mer herdbart enn a.
For å oppsummere: normalisering og utgløding er veldig like prosesser som ofte forveksles. Forvekslingen er ikke veldig farlig, men det er absolutt en forskjell mellom prosessene, både i utførelse og behov. Begge gjøres for å mykne opp og “tilbakestille“ stålet til en tilstand som er enklere å bearbeide, men utgløding brukes hovedsakelig der termisk bearbeiding har endret sammensetningen av krystallene, mens normalisering benyttes når mekanisk bearbeiding har innført forskyvninger og stress i kornstrukturen.
Settherding og flammerherding
Settherding og flammerherding er begge karburiserende prosesser, og like i det at det er hovedsakelig en overflatebehandling, men de varierer noe i utførelse.
I situasjoner der vi kun behøver et veldig hardt ytre, kan vi tilføre karbon til stålet slik at overflaten inneholder mer karbon og derfor blir mye hardere ved herding. Gjennomherding er nødvendig når delen skal brukes i applikasjoner der energien forplantes gjennom hele delen, som f.eks. en hammer, mens settherding er nyttig når vi trenger en slitesterk overflate med en sterk kjerne, som en drivaksling.
Settherding med Kasenit
Idéen er å la stålet ligge oppvarmet i en karbon-rik atmosfære. Varmen tillater stålet å suge til seg karbon fra omgivelsene. Dette kan gjøres i ovn, men en annen mye brukt metode er herdepulver, et kjent merke er “Kasenit”, men dette selges ikke lenger. Det finnes et substitutt kalt “Cherry Red“.
Dette er et pulver som inneholder amorft karbon og andre elementer som gjør at det smelter og pakker seg som en klump rundt en oppvarmet bit med stål når det dyppes i det. Delen dynkes fullstendig i pulveret, tas opp, og varmes en liten stund innkapslet i pulveret. Grunnen til at pulveret smelter og lager en slags kokong rundt stålet er for å hindre tilgangen på oksygen, som vil motvirke prosessen. Delen kan og bør dynkes flere ganger. Delen bråkjøles så i en passende kjølevæske, vanligvis vann. Denne prosessen er ofte brukt på mindre deler. Det er også mulig å legge delen i et bad av pulveret og varme opp hele badet i en lengre periode, dette kan gi bedre resultater.
Stålet kan også karburiseres, kjøles ned, maskineres og så herdes slik at kun noen områder blir harde. Delen kan også slipes etter at den er herdet, men dette krever at stålet for nok tid til å bygge et tykt høy-karbon skall. Settherdede deler behøver vanligvis ikke anløpes til samme grad som gjennomherdet stål, og i noen situasjoner er det nødvendig å ikke anløpe i det hele tatt. Kjernen vil fremdeles være mykere og sterkere etter herding p.g.a. det lavere karboninnholdet.
Vi kan se av grafen over at stålet må ligge i ganske mange timer for å bygge et tykt lag. Høyere temperaturer fremskynder prosessen. For at vi skal ha noe som helst håp om å oppnå slike tider må vi bruke en ovn.
Å hindre oksygentilførsel er the name of the game, og ved bruk av ovn er det nødvendig å pakke inn delen i en lufttett boks eller lignende og forsegle alle åpninger. Delen legges i boksen, omringet av karburiserende materiale, f.eks. kull eller trekull, knust relativt fint. Bruk av kun kull funker, men er en ganske treg prosess, vi kan effektivisere den ved å blande inn natriumkarbonat, eller litt settherdingspulver, ca 1-5% vekt.
Boksen varmes opp med ovnen og blir liggende ved 880-920°C til ønsket tykkelse er oppnådd. Boksen kjøles ned igjen og kan deretter herdes på normalt vis. Delen trenger ikke være på herdetemperatur lenge ved herding av settherdede deler.
Det kan være lurt å legge ved en liten offer-bit for å teste hardheten uten å prøve å file på selve delen.
Flammeherding går ut på mye av det samme, men gjøres hovedsakelig av kosmetiske årsaker:
I flammeherding brukes det organisk karbon, som beinkull, lær og den slags og bitene kan være større. Effekten blir sterkere der stålet har vært i nærmere kontakt med kullbitene, så å ha litt størrelse på dem fremhever forskjellene.
Ved flammeherding må delene bråkjøles rett fra boksen, uten å få tilgang til oksygen i mellomtiden, som kan være en utfordring, men metoden er vanligvis å feste lokket med ståltråd og senke boksen opp ned i en tønne med vann og klippe tråden slik at delene detter ut av boksen og synker direkte ned i vannet.
Settherding i boks gir et tykkere karbonlag, men fordelen med pulver-metoden er at krystallene ikke får samme mulighet til å gro, men dette er vanligvis ikke et problem.
Det var siste kapittel i serien om stål. Jeg håper det har gitt et innblikk i metallurgiens verden og en oversikt og generell forståelse for hvordan stål oppfører seg, og hvorfor vi behandler det som vi gjør. Det var en monumental oppgave å kondensere all denne informasjonen til noe fordøyelig, og det er bare toppen av isfjellet om man virkelig vil dykke dypere ned i dette, men jeg håper det er en god start. Jeg forsøker å begrense omfanget av innleggene mine, så forvent kortere, men til gjengjeld flere, innlegg i 2020.
Godt nyttår!